Twee baanbrekende onderzoekers hebben de $3 miljoen Breakthrough Prize in Life Sciences ontvangen voor hun fundamentele werk op het gebied van genbewerking. Dr. Swee Lay Thein van het National Heart, Lung, and Blood Institute (NHLBI) en Dr. Stuart H. Orkin van de Harvard University zijn erkend voor het fundamentele onderzoek dat de weg vrijmaakte voor Casgevy, de eerste goedgekeurde therapie die CRISPR-technologie gebruikt voor de behandeling van sikkelcelziekte en bèta-thalassemie.
De wetenschap van het ‘onderdrukken van de onderdrukker’
Het pad naar deze medische mijlpaal begon met een fundamentele vraag: waarom ervaren sommige patiënten met bloedaandoeningen veel mildere symptomen dan andere?
Decennia lang hebben wetenschappers een biologisch fenomeen waargenomen waarbij hemoglobine betrokken was: het molecuul in de rode bloedcellen dat verantwoordelijk is voor het transport van zuurstof. Mensen produceren twee hoofdtypen:
1. Foetale hemoglobine: Geproduceerd in de baarmoeder.
2. Volwassen hemoglobine: Neemt het over na de geboorte.
Bij de meeste mensen “schakelt” het lichaam de productie van foetaal hemoglobine uit naarmate ze ouder worden. Uit het onderzoek van Dr. Thein naar grote familielijnen bleek echter dat sommige individuen een genetische eigenaardigheid bezaten waardoor ze hun hele leven hoge niveaus van foetaal hemoglobine konden blijven produceren.
Door middel van gedetailleerde genetische analyse identificeerde haar team een specifiek gen op chromosoom 11, genaamd BCL11A. Dit gen fungeert als een ‘repressor’; het is zijn taak de foetale hemoglobineproductie uit te schakelen. Het onderzoek van Dr. Orkin bewees dat door het gebruik van hulpmiddelen voor het bewerken van genen om deze repressor aan te pakken en uit te schakelen, wetenschappers het lichaam in wezen konden ‘misleiden’ om de foetale hemoglobineproductie actief te houden.
Van genetische ontdekking tot een ‘functioneel geneesmiddel’
De toepassing van deze ontdekking leidde tot de ontwikkeling van Casgevy, een behandeling waarbij gebruik wordt gemaakt van CRISPR ‘moleculaire scharen’ om de eigen cellen van een patiënt te bewerken. Het proces is zeer geavanceerd:
– Extractie: Beenmergstamcellen worden uit de patiënt verwijderd.
– Bewerking: CRISPR wordt gebruikt om het BCL11A-repressorgebied eruit te halen.
– Herinfusie: De bewerkte cellen worden terug in de patiënt geïnjecteerd, waar ze gezonde, zuurstofdragende rode bloedcellen beginnen te produceren.
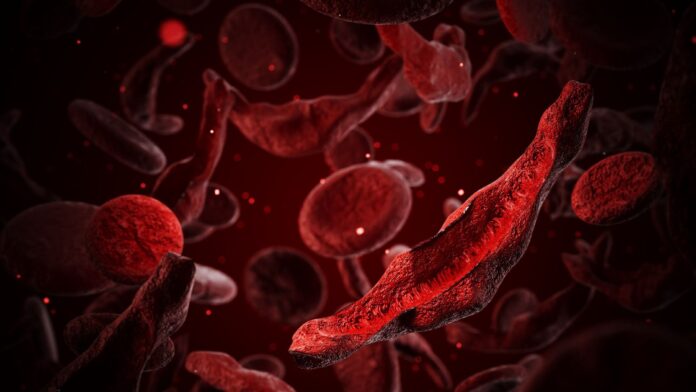
Voor patiënten met sikkelcelziekte – die wereldwijd zeven tot acht miljoen mensen treft – is dit een transformatieve ontwikkeling. Bij sikkelcelziekte vervormen rode bloedcellen zich tot halvemaanvormige vormen, wat ondragelijke pijn, orgaanschade en levensbedreigende blokkades veroorzaakt. Door het foetale hemoglobine te herstellen, biedt Casgevy wat wordt beschreven als een “functionele genezing.”
Uitdagingen: toegankelijkheid en de weg die voor ons ligt
Ondanks de wetenschappelijke triomf wordt de huidige implementatie van CRISPR-therapie geconfronteerd met aanzienlijke hindernissen die verhinderen dat het een universele oplossing is.
1. De fysieke en financiële tol
Het behandelproces is ongelooflijk belastend. Patiënten moeten zware chemotherapie ondergaan om hun beenmerg voor te bereiden op de nieuwe cellen, een proces dat wel een jaar kan duren. Bovendien lopen de kosten van de therapie in de miljoenen dollars, waardoor deze voor een groot deel van de wereldbevolking ontoegankelijk wordt.
2. De geografische kloof
Sikkelcelziekte en bèta-thalassemie komen het meest voor in Afrika, Azië en het Middellandse Zeegebied – regio’s waar vaak de hightech medische infrastructuur ontbreekt die nodig is voor complexe beenmergtransplantaties en genbewerking.
3. De zoektocht naar eenvoudigere oplossingen
Om deze kloof te overbruggen, kijkt de wetenschappelijke gemeenschap naar twee belangrijke grenzen:
– “In vivo”-bewerking: Ontwikkeling van methoden om machines voor genbewerking rechtstreeks in de patiënt te injecteren, waardoor de noodzaak voor beenmergextractie en -herinfusie wordt geëlimineerd.
– Farmacologische alternatieven: Onderzoek naar medicijnen zoals Mitavipat, dat tot doel heeft de metabolische gezondheid van rode bloedcellen te verbeteren, en mogelijk een veel goedkopere en gemakkelijker toe te dienen optie biedt via pillen of infusies.
De Breakthrough Prize erkent een monumentale sprong in de genetische geneeskunde, maar de volgende grote uitdaging ligt in het toegankelijk en betaalbaar maken van deze levensreddende technologieën voor de miljoenen die ze het meest nodig hebben.
Conclusie
Terwijl de erkenning van Dr. Thein en Dr. Orkin een historische overwinning markeert voor genbewerking, verschuift de focus van de medische gemeenschap nu van het bewijzen van de wetenschap naar het oplossen van de logistieke en economische barrières van de mondiale gezondheidszorg.