Dois pesquisadores pioneiros receberam o Prêmio Revelação de US$ 3 milhões em Ciências da Vida por seu trabalho fundamental na edição de genes. Swee Lay Thein, do Instituto Nacional do Coração, Pulmão e Sangue (NHLBI), e o Dr. Stuart H. Orkin, da Universidade de Harvard, foram reconhecidos pela pesquisa básica que abriu o caminho para Casgevy, a primeira terapia aprovada usando a tecnologia CRISPR para tratar a doença falciforme e a beta-talassemia.
A Ciência de “Reprimir o Repressor”
O caminho para este marco médico começou com uma questão fundamental: Porque é que alguns pacientes com doenças sanguíneas apresentam sintomas muito mais ligeiros do que outros?
Durante décadas, os cientistas observaram um fenómeno biológico envolvendo a hemoglobina – a molécula dos glóbulos vermelhos responsável pelo transporte de oxigénio. Os humanos produzem dois tipos principais:
1. Hemoglobina fetal: Produzida no útero.
2. Hemoglobina adulta: assume o controle após o nascimento.
Na maioria das pessoas, o corpo “desliga” a produção de hemoglobina fetal à medida que amadurecem. No entanto, a pesquisa do Dr. Thein sobre grandes linhagens familiares revelou que alguns indivíduos possuíam uma peculiaridade genética que lhes permitia continuar a produzir altos níveis de hemoglobina fetal ao longo da vida.
Através de análises genéticas detalhadas, sua equipe identificou um gene específico no cromossomo 11 chamado BCL11A. Este gene atua como um “repressor” – sua função é desligar a produção de hemoglobina fetal. A pesquisa do Dr. Orkin provou que, ao usar ferramentas de edição genética para atingir e desativar esse repressor, os cientistas poderiam essencialmente “enganar” o corpo para manter ativa a produção de hemoglobina fetal.
Da descoberta genética a uma “cura funcional”
A aplicação desta descoberta levou ao desenvolvimento do Casgevy, um tratamento que utiliza “tesouras moleculares” CRISPR para editar as células do próprio paciente. O processo é altamente sofisticado:
– Extração: Células-tronco da medula óssea são removidas do paciente.
– Edição: CRISPR é usado para cortar a região do repressor BCL11A.
– Reinfusão: As células editadas são infundidas de volta no paciente, onde começam a produzir glóbulos vermelhos saudáveis e transportadores de oxigênio.
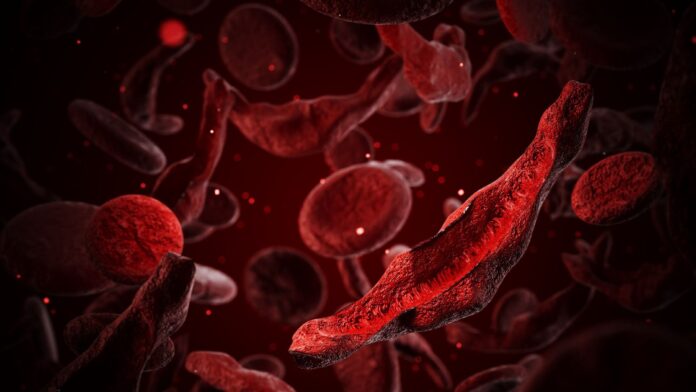
Para os pacientes com doença falciforme – que afecta 7 a 8 milhões de pessoas em todo o mundo – este é um desenvolvimento transformador. Na doença falciforme, os glóbulos vermelhos se deformam em forma de lua crescente, causando dor insuportável, danos a órgãos e bloqueios com risco de vida. Ao restaurar a hemoglobina fetal, Casgevy fornece o que é descrito como uma “cura funcional”.
Desafios: Acessibilidade e o futuro
Apesar do triunfo científico, a implementação atual da terapia CRISPR enfrenta obstáculos significativos que a impedem de ser uma solução universal.
1. O tributo físico e financeiro
O processo de tratamento é incrivelmente desgastante. Os pacientes devem ser submetidos a quimioterapia rigorosa para preparar a medula óssea para as novas células, um processo que pode levar até um ano. Além disso, o custo da terapia chega a milhões de dólares, tornando-a inacessível para grande parte da população global.
2. A lacuna geográfica
A doença falciforme e a beta-talassemia são mais prevalentes em África, na Ásia e no Mediterrâneo – regiões que muitas vezes carecem da infra-estrutura médica de alta tecnologia necessária para transplantes complexos de medula óssea e edição genética.
3. A busca por soluções mais simples
Para colmatar esta lacuna, a comunidade científica procura duas fronteiras principais:
– Edição “in vivo”: Desenvolvimento de métodos para injetar máquinas de edição genética diretamente no paciente, eliminando a necessidade de extração e reinfusão de medula óssea.
– Alternativas farmacológicas: Pesquisar medicamentos como o Mitavipat, que visa melhorar a saúde metabólica dos glóbulos vermelhos, oferecendo potencialmente uma opção muito mais barata e de administração mais fácil por meio de comprimidos ou infusões.
O Prémio Breakthrough reconhece um salto monumental na medicina genética, mas o próximo grande desafio reside em tornar estas tecnologias que salvam vidas acessíveis e acessíveis aos milhões que mais necessitam delas.
Conclusão
Embora o reconhecimento do Dr. Thein e do Dr. Orkin marque uma vitória histórica para a edição genética, o foco da comunidade médica está agora a mudar da comprovação da ciência para a resolução das barreiras logísticas e económicas da prestação global de cuidados de saúde.