Deux chercheurs pionniers ont reçu le Prix Breakthrough de 3 millions de dollars en sciences de la vie pour leurs travaux fondamentaux en matière d’édition génétique. Le Dr Swee Lay Thein du National Heart, Lung, and Blood Institute (NHLBI) et le Dr Stuart H. Orkin de l’Université Harvard ont été récompensés pour leurs recherches fondamentales qui ont ouvert la voie à Casgevy, la première thérapie approuvée utilisant la technologie CRISPR pour traiter la drépanocytose et la bêta-thalassémie.
La science de la « répression du répresseur »
Le chemin menant à cette étape médicale a commencé par une question fondamentale : pourquoi certains patients atteints de troubles sanguins présentent-ils des symptômes beaucoup plus légers que d’autres ?
Pendant des décennies, les scientifiques ont observé un phénomène biologique impliquant l’hémoglobine, la molécule présente dans les globules rouges responsable du transport de l’oxygène. Les humains produisent deux types principaux :
1. Hémoglobine fœtale : Produite dans l’utérus.
2. Hémoglobine adulte : Prend le relais après la naissance.
Chez la plupart des gens, le corps « arrête » la production d’hémoglobine fœtale à mesure qu’ils mûrissent. Cependant, les recherches du Dr Thein sur les grandes lignées familiales ont révélé que certains individus possédaient une particularité génétique qui leur permettait de continuer à produire des niveaux élevés d’hémoglobine fœtale tout au long de leur vie.
Grâce à une analyse génétique détaillée, son équipe a identifié un gène spécifique sur le chromosome 11 appelé BCL11A. Ce gène agit comme un « répresseur » : son rôle est de désactiver la production d’hémoglobine fœtale. Les recherches du Dr Orkin ont prouvé qu’en utilisant des outils d’édition génétique pour cibler et désactiver ce répresseur, les scientifiques pouvaient essentiellement « tromper » le corps pour qu’il maintienne active sa production d’hémoglobine fœtale.
De la découverte génétique à une « guérison fonctionnelle »
L’application de cette découverte a conduit au développement de Casgevy, un traitement qui utilise les « ciseaux moléculaires » CRISPR pour modifier les propres cellules d’un patient. Le processus est très sophistiqué :
– Extraction : Les cellules souches de la moelle osseuse sont prélevées sur le patient.
– Édition : CRISPR est utilisé pour supprimer la région du répresseur BCL11A.
– Réinfusion : Les cellules modifiées sont réinjectées dans le patient, où elles commencent à produire des globules rouges sains et porteurs d’oxygène.
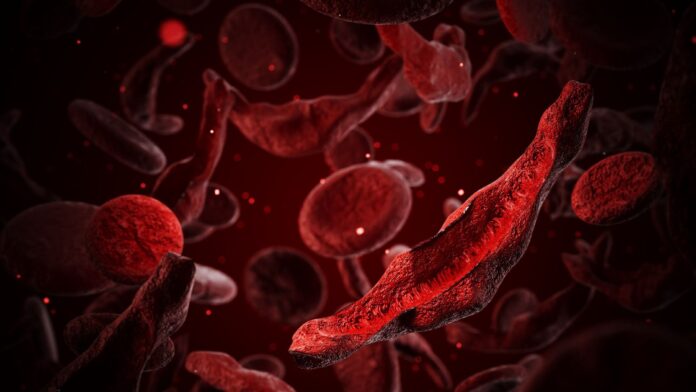
Pour les patients atteints de drépanocytose, qui touche 7 à 8 millions de personnes dans le monde, il s’agit d’une évolution transformatrice. Dans la drépanocytose, les globules rouges se déforment en forme de croissant, provoquant des douleurs atroces, des lésions organiques et des blocages potentiellement mortels. En restaurant l’hémoglobine fœtale, Casgevy offre ce qui est décrit comme une ** « guérison fonctionnelle ».**
Défis : accessibilité et chemin à parcourir
Malgré le triomphe scientifique, la mise en œuvre actuelle de la thérapie CRISPR se heurte à des obstacles importants qui l’empêchent de constituer une solution universelle.
1. Le bilan physique et financier
Le processus de traitement est incroyablement éprouvant. Les patients doivent subir une chimiothérapie sévère pour préparer leur moelle osseuse aux nouvelles cellules, un processus qui peut prendre jusqu’à un an. De plus, le coût de la thérapie s’élève à des millions de dollars, ce qui la rend inaccessible à une grande partie de la population mondiale.
2. L’écart géographique
La drépanocytose et la bêta-thalassémie sont les plus répandues en Afrique, en Asie et dans les régions méditerranéennes, régions qui manquent souvent de l’infrastructure médicale de haute technologie requise pour les greffes complexes de moelle osseuse et l’édition génétique.
3. La recherche de solutions plus simples
Pour combler ce fossé, la communauté scientifique se tourne vers deux frontières principales :
– Édition « in vivo » : Développement de méthodes permettant d’injecter des machines d’édition de gènes directement dans le patient, éliminant ainsi le besoin d’extraction et de réinfusion de moelle osseuse.
– Alternatives pharmacologiques : Recherche de médicaments comme Mitavipat, qui vise à améliorer la santé métabolique des globules rouges, offrant potentiellement une option beaucoup moins chère et plus facile à administrer via des pilules ou des perfusions.
Le Breakthrough Prize récompense une avancée monumentale dans le domaine de la médecine génétique, mais le prochain grand défi consiste à rendre ces technologies vitales accessibles et abordables aux millions de personnes qui en ont le plus besoin.
Conclusion
Alors que la reconnaissance du Dr Thein et du Dr Orkin marque une victoire historique pour l’édition génétique, l’attention de la communauté médicale passe désormais de la preuve scientifique à la résolution des obstacles logistiques et économiques de la prestation de soins de santé à l’échelle mondiale.