Двое выдающихся исследователей были удостоены премии Breakthrough Prize в области наук о жизни в размере 3 миллионов долларов за их фундаментальный вклад в развитие технологии редактирования генов. Доктор Сви Лей Тейн из Национального института сердца, легких и крови (NHLBI) и доктор Стюарт Х. Оркин из Гарвардского университета получили признание за базовые исследования, которые проложили путь к созданию Casgevy — первой одобренной терапии с использованием технологии CRISPR для лечения серповидноклеточной анемии и бета-талассемии.
Наука «подавления подавителя»
Путь к этому медицинскому достижению начался с фундаментального вопроса: почему у одних пациентов с заболеваниями крови симптомы протекают гораздо легче, чем у других?
На протяжении десятилетий ученые наблюдали биологический феномен, связанный с гемоглобином — молекулой в эритроцитах, отвечающей за перенос кислорода. У людей вырабатываются два основных типа гемоглобина:
1. Фетальный гемоглобин: вырабатывается в утробе матери.
2. Взрослый гемоглобин: берет на себя функции после рождения.
У большинства людей по мере взросления организм «отключает» производство фетального гемоглобина. Однако исследования доктора Тейн, изучавшей обширные семейные родословные, показали, что некоторые люди обладают генетической особенностью, которая позволяет им поддерживать высокий уровень фетального гемоглобина на протяжении всей жизни.
Благодаря детальному генетическому анализу ее команда идентифицировала специфический ген в 11-й хромосоме под названием BCL11A. Этот ген действует как «репрессор» — его задача заключается в том, чтобы прекратить выработку фетального гемоглобина. Исследования доктора Оркина доказали, что с помощью инструментов редактирования генов можно воздействовать на этот репрессор и отключить его, фактически «обманув» организм и заставив его продолжать вырабатывать фетальный гемоглобин.
От генетического открытия к «функциональному излечению»
Применение этого открытия привело к разработке Casgevy — метода лечения, который использует «молекулярные ножницы» CRISPR для редактирования собственных клеток пациента. Процесс крайне сложен:
– Экстракция: у пациента извлекаются стволовые клетки костного мозга.
– Редактирование: с помощью CRISPR вырезается область репрессора BCL11A.
– Реинфузия: отредактированные клетки вводятся обратно пациенту, где они начинают вырабатывать здоровые, способные переносить кислород эритроциты.
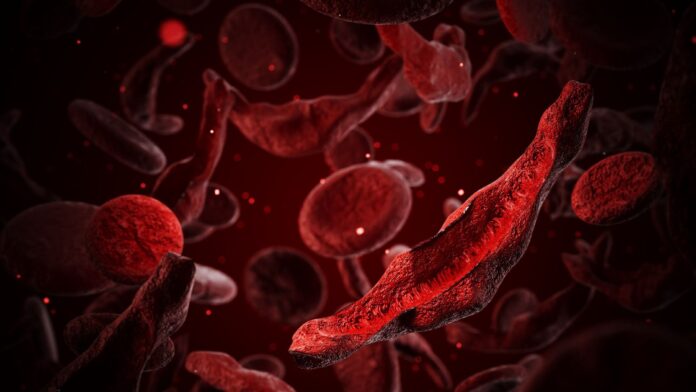
Для пациентов с серповидноклеточной анемией, которой во всем мире страдают от 7 до 8 миллионов человек, это событие имеет трансформирующее значение. При этом заболевании эритроциты деформируются, принимая форму серпа, что вызывает невыносимую боль, повреждение органов и опасные для жизни закупорки сосудов. Восстанавливая уровень фетального гемоглобина, Casgevy обеспечивает то, что называют «функциональным излечением».
Проблемы: доступность и путь вперед
Несмотря на научный триумф, нынешнее внедрение терапии CRISPR сталкивается со значительными препятствиями, которые мешают ей стать универсальным решением.
1. Физическая и финансовая нагрузка
Процесс лечения невероятно изнурителен. Пациенты должны пройти через жесткую химиотерапию, чтобы подготовить костный мозг к принятию новых клеток — этот процесс может занимать до года. Более того, стоимость терапии исчисляется миллионами долларов, что делает её недоступной для большей части населения планеты.
2. Географический разрыв
Серповидноклеточная анемия и бета-талассемия наиболее распространены в Африке, Азии и Средиземноморском регионе — в регионах, где зачастую отсутствует высокотехнологичная медицинская инфраструктура, необходимая для сложных трансплантаций костного мозга и редактирования генов.
3. Поиск более простых решений
Чтобы преодолеть этот разрыв, научное сообщество ориентируется на два основных направления:
– Редактирование in vivo : разработка методов введения механизмов редактирования генов непосредственно в организм пациента, что исключит необходимость извлечения и повторного введения костного мозга.
– Фармакологические альтернативы: исследование таких препаратов, как Mitavipat, целью которых является улучшение метаболического здоровья эритроцитов. Это потенциально может предложить гораздо более дешевый и простой вариант применения в виде таблеток или инфузий.
Премия Breakthrough Prize отмечает колоссальный скачок в генетической медицине, однако следующая великая задача заключается в том, чтобы сделать эти спасительные технологии доступными и недорогими для миллионов людей, которые нуждаются в них больше всего.
Заключение
Хотя признание заслуг доктора Тейн и доктора Оркина знаменует собой историческую победу генного редактирования, внимание медицинского сообщества теперь смещается от доказательства научной состоятельности к решению логистических и экономических барьеров в мировом здравоохранении.